מה זה IVDR
- IVDR היא הרגולציה החדשה של האיחוד האירופי החלה על מכשירים רפואיים דיאגנוסטים (מכשור מעבדה).
- ה-IVDR נוצר כדי להבטיח התאמה לכל מכשור המעבדה הדיאגנוסטי (IVD , in vitro diagnostic) המשמשים באיחוד האירופי וחלים על כל IVD.
- בעקבות כניסת ה- IVDR , רבים ממכשירי ה IVD צפויים להיות מסווגים מחדש, ולדרוש בדיקת גוף מוסמך (Notified Body).
עיכובים צפויים במעבר ל-IVDR
כ-90% מהמכשירים הדיאגנוסטיים ידרשו לעבור סקירה ע” גופים מוסמכים Notified Body.
התהליך ישפיע על מסמכים רגולטורים, נתונים קליניים של החברה והאופן בו הם נאספים, QMS מערכת האיכות של החברה (QMS- Quality Management System), וולידציות.
לוחות הזמנים עלולים להיות מושפעים מעיכובים הצפויים במעבר ל-IVDR , עקב העומסים על הגופים מוסמכים שהוסמכו לאשר מוצרים תחת ה-IVDR.
- כל המוצרים שהיו עד היום תחת IVDD (In-Vitro Device Directive) ידרשו בסופו של דבר לעבור הסמכה תחת IVDR.
- לא כל ה Notified Body שהוסמכו ל- IVDD יורשו להעביר הסמכה ל- IVDR.
- על היצרנים יש לעדכן את התיק הטכני (Technical File) ולהתאים לחקיקה החדשה עד למועד היישום של ה- IVDR ב -25 במאי 2022.
תהליכי מפתח שיש לקחת בחשבון ב- QMS שלך
בנוסף לתהליכים רגולטוריים, תהליכים קליניים, הבטחת איכות, ולידציה והנדסה, ה- IVDR שם דגש על ממשקים שונים של מערכת האיכות.

Regulatory Affairs - תהליכים רגולטוריים בהקשר ל- IVDR
- לפי IVDR- יש דרישה לבניית אסטרטגיה רגולטורית, ולהבין את ההשפעה על המוצרים שלך.
- יש לאסוף נתוני הערכת ביצועים (performance evaluation) שתומכים בהתוויית השימוש שלכם- עבור המוצר שנמצא כבר בשוק (אם המוצר הוא Self-declared).
- יש לשקול את היעילות והבטיחות של מוצרים מיושנים.
- שימו לב: בין אם הנתונים נאספו ע”י החברה שלכם או גוף שלישי- יש לוודא אמינות ושלמות של הנתונים. יש לשקול האם אתם מסוגלים להעביר את הנתונים והאם כדאי לכם להגיש את המוצר מחדש תחת הIVDR.
- מומלץ לעשות סקירה של מסמכי הפיתוח מנקודת מבט של רגולציה- לצורך הגשת המוצר לרשויות, החברה צריכה תיק פיתוח ותיק ייצור מלאים מעודכנים ועומדים בדרישות.
- יש לעדכן את הערכת סיכונים לפי דרישות ה- IVDR ו- ISO14791:2019.
- יש להגדיר אחראי על תאימות לתקנות (Person Responsible for Regulatory Compliance- PPRC) עם ניסיון רלוונטי, יכול להיות פנים ארגוני או לקבל את השרות ע”י יועץ חיצוני .
- וכמובן, לכתוב ולנהל את מסמכי ההגשה והתיק הטכני של המוצר לפי הרגולציה החדשה.
Contact us and we will be happy to meet and assist you with your needs
דרישות עבור Own Brand Labeling (OBL)
- אותם דרישות כמו OEM
- גישה לתיק הטכני, כולל ולידציה של סטריליזציה שנעשה ע”י קבלן-משנה של OEM
- גישה לנתוני PMS (Post Market Surveillance)
- ביקורת מלאה של שרשרת האספקה
- בפועל OBL הופך ליצרן חוקי!
Clinical affairs and PMS
- נתונים קליניים נוספים ידרשו כדי לענות על החקיקה החדשה IVDR.
- כמו כן, יש לעדכן את התוכניות והדוחות של ה- Post Market Surveillance (PMS) בהתאם לדרישות החדשות.
- עדכון דוח הערכת הביצועים Performance Evaluation Report (PER) בעקבות הדרישות חדשות של IVDR
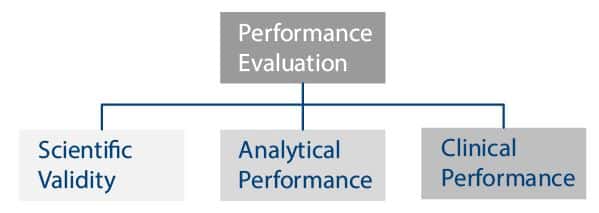
- Scientific Validity Report או דוח תוקף מדעי שכולל סקירה ספרותית- למשל אם הגשתם את המוצר שלכם לפני 5 שנים, יתכן ויש מאמרים חדשים שתומכים בהתוויה של המוצר, או להפך. IVDR Annex XIII, part A
דוח התוקף המדעי (Scientific Validity Report)- אם החברה מכניסה מוצר חדש לשוק, חשוב שתתחיל את הסקירה בשלב מוקדם של מחזור החיים של מכשיר ה IVD. אחת הדרכים לעשות זאת היא להשתמש במידע רלוונטי על תוקפו המדעי של מכשירים המודדים את אותו אנליט או סמן. אפשר, וחובה, לבצע חיפוש מפורט בספרות, אך אם אין הוכחות מספקות החברה תידרש לבצע הוכחת היתכנות קלינית, מחקרים פרה-קליניים או מחקרי ביצועים קליניים. כל הממצאים שלך יסוכמו בדוח התוקף המדעי שיהפוך לחלק מדוח הערכת הביצועים (Performance Evaluation).
- Analytical Performance Report– מתאר את מאפייני המוצר. אלה כוללים רגישות, ספציפיות, הדירות, שחזור, ועוד. יש לשמור את הרישומים של מאפייני הביצועים אלה לאורך חיי המכשיר. התוצאה של הביצועים האנליטיים אלו יסוכמו בדוח ביצועים אנליטיים. ראה סעיף 9.1 של Annex I ב-IVDR.
- Clinical Performance Report– ניתוח של הביצועים הקליניים. המיקוד כאן הוא מדידת הדיוק האבחוני של המכשיר. במקרים רבים יהיה אפשרי לערוך מחקר ביצועים קליניים רטרוספקטיבי(שימוש בדוגמאות קיימות) במקום לבצע מחקר קליני פרוספקטיבי (דוגמאות יעודיות עבור ניסוי ספציפי).
המלצה: אם אתם בשלב איסוף נתונים עם המכשיר שלך, בין אם זה לניסויים קלינים או להגשות למדינות אחרות, יש לשקול איך להשתמש בהם להכנת PER במסגרת הסמכה ל-IVDR
הבטחת איכות Quality Assurance (QA)
יש לבצע הערכת פערים- Gap Assessment של המערכת איכות לפי הרישות ה-IVDR, לעדכן מסמכים ותהליכים, וליישם את העדכונים החדשים. הסיבה לכך:
- IVDR מגדיר דרישות ספציפיות עבור QMS (Article 10(8); Obligations of manufacturer).
- הדרישות של IVDR אינן זהות לחלוטין לאלו של ISO13485:2016.
כמו כן יש להתייעץ עם גוף הסמכה ל-ISO 13485:2016 שלך לווידוא התאמת המערכת QMS לחקיקה החדשה של IVDR.
- חשוב: מומלץ לדון עם הגוף שמסמיך את החברה לISO 13485:2016, אם הוא מוכר על ידי Notified Body שמאושר לאשר מוצרים במסגרת ה-IVDR. אם כן, הכרה-הדדית כזו יכולה לזרז ולהקל על תהליכי ההטמעה.
וולידציה
- יש לעשות סקירה של נתונים אנליטים ונתוני הביצוע עבור המכשיר שלכם ולהבטיח שהוא עומד בדרישות החדשות.
- דרישות ולידציה מפורטות ב-IVDR Technical File format.
- IVDR מגדיר General Safety and Performance Requirements (GSPR), לעומת Essential requirements שהיו ב-IVDD. היות וחלק מהדרישות מפורטות יותר, או שונות מאלו שהיו בדירקטיבה IVDD- יש לבנות תוכנית איך מגשרים על הפער הזה. השינויים יכולים לכלול את תוכנית הוולידציה- VMP, אספקטים אחרים יכולים להיות קשורים ל-IQ/OQ/PQ, ולידצית שילוח, וולידציית תהליך, ולידציית מערכות ממוחשבות (chi אם מדובר על התוכנה של המכשיר עצמו, או תוכנה שתומכת בייצור של המכשיר).
הנדסה
- יש להיערך לקראת UDI (Unique Device Identification)- עקיבות של המוצרים לאירופה. התהליך דומה לדרישות ארה”ב, עם תוספת של פרטים מסויימים (Basic UDI-DI).
- כמו כן, מומלץ להתייחס לדרישות IVDR אם אתם בתהליך NPI (New Product Introduction) או מתכננים תהליך גמלון ולוודא שאתם אכן עומדים בדרישות רגולטוריות חדשות.
איך נוכל לעזור?
חברת RS-NESS תעזור לכם בביצוע IVDR Gap Assessment, לבנות תוכנית עבודה לפרויקט ולעזור ליישם את התוכנית בדרך להסמכה שלכם ל-IVDR בכל ההיבטים שהוזכרו במאמר: בתחום האיכות QA, רגולציה RA , קליניקה CA , וולידציה, הנדסה וניהול פרויקטים.
About the Author

Yael Himmel Shlomo
Director of Regulatory Affairs
Yael is experienced in leading regulatory processes in companies in different stages, managing and mitigating risks, and carrying discussions with different regulatory agencies. She helps our clients mitigate regulatory risks and navigate regulatory complexities, and develop regulatory strategies that go hand-in-hand with the client’s business strategies.


















